Régulation de la nucléation des microtubules

Paul CONDUIT
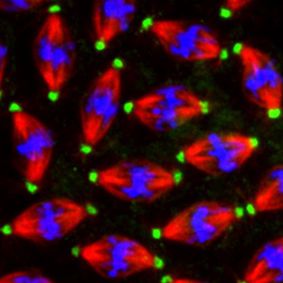
Nous voulons acquérir une compréhension fondamentale de la manière dont la nucléation des microtubules est régulée spatio-temporellement dans le contexte des animaux pluricellulaires.
Nous sommes particulièrement intéressés par la façon dont les mécanismes régulant la formation et l’organisation des microtubules varient entre les types de cellules, y compris dans les cellules en division et les neurones.
Mots-clés : Microtubules, division cellulaire, neurones, gamma-tubuline, g-TuRC, MTOC, centrosome, drosophile
+33 (0)1 57 27 80 95 Contact @pconduit.bsky.social
Objectif de la recherche
Nous voulons acquérir une compréhension fondamentale de la façon dont la nucléation des microtubules est régulée spatio-temporellement dans le contexte d’animaux multicellulaires. Nous nous intéressons particulièrement à la manière dont les mécanismes de régulation de la formation et de l’organisation des microtubules varient selon les types de cellules.
Background
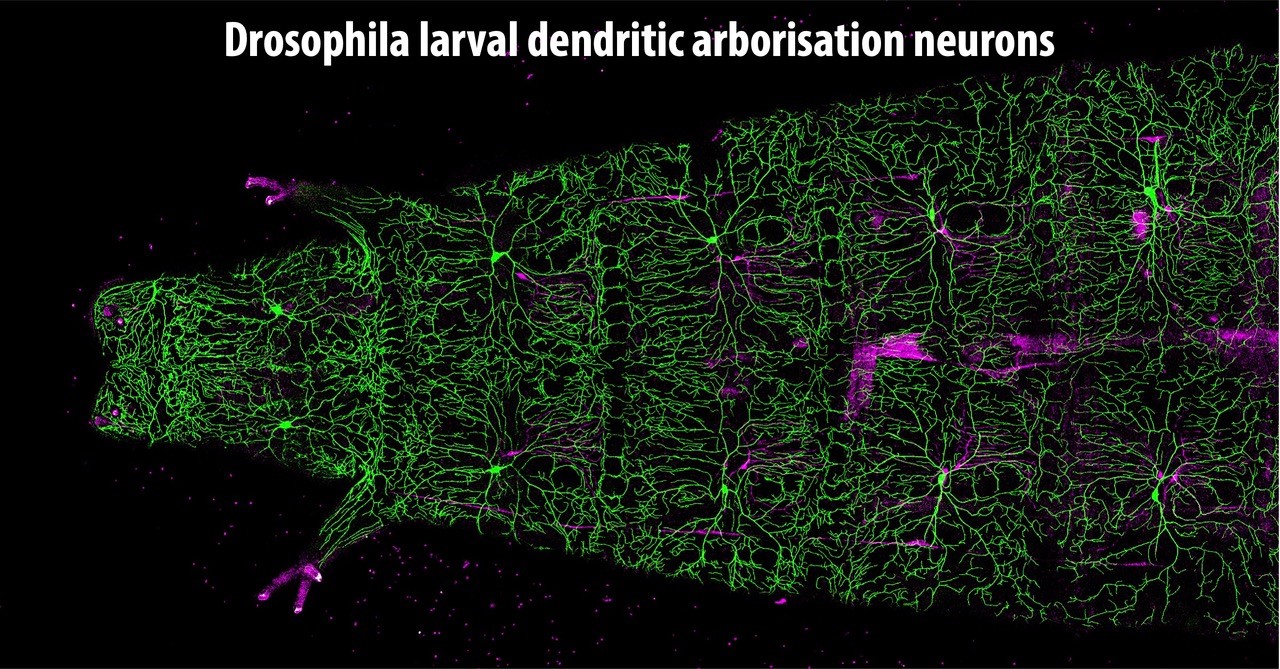
Les microtubules sont des polymères dynamiques qui font partie du cytosquelette de la cellule. Ils forment une variété spectaculaire de tableaux à travers différents types de cellules et stades de développement. Par exemple, pendant la division cellulaire, les microtubules sont disposés dans le fuseau mitotique, qui sépare les chromosomes dupliqués de manière égale entre les cellules filles. Dans les neurones matures, cependant, les microtubules sont disposés en réseaux polarisés qui traversent les axones et les dendrites. Ces réseaux sont nécessaires pour le soutien structurel, la croissance des neurites et le transport des molécules entre le corps cellulaire et les terminaisons des neurites. Toutes les cellules utilisent la même machinerie fondamentale pour générer et organiser les microtubules, alors comment différentes cellules forment-elles des réseaux de microtubules aussi différents?
Programme de recherche
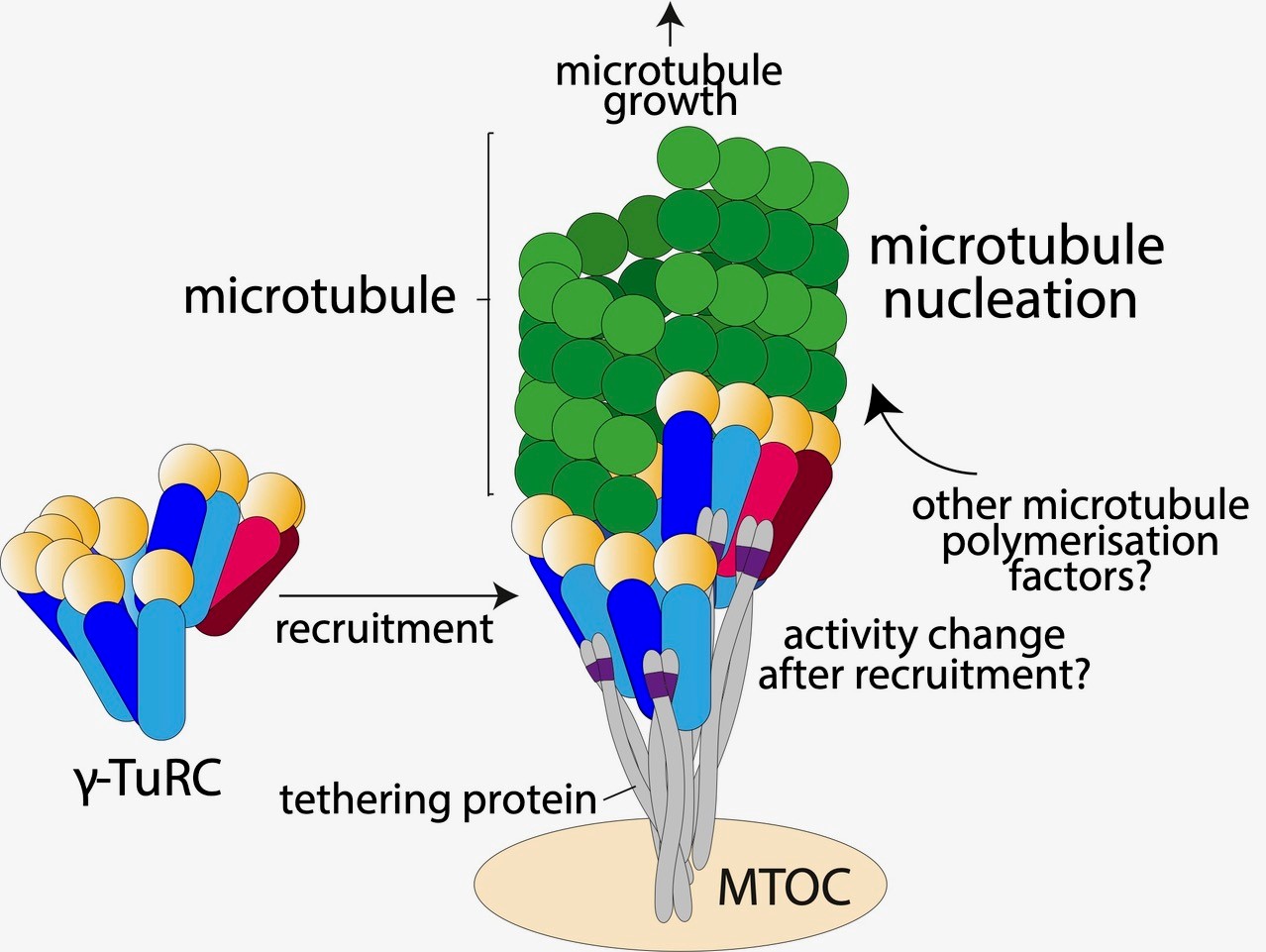
Nous abordons cette question en étudiant la régulation moléculaire des γ-tubulin ring complexes (γ-TuRCs), qui modélisent et catalysent la formation de microtubules de novo. Les γ-TuRC sont recrutés et activés à des sites spécifiques au sein des cellules afin de générer de nouveaux microtubules au bon endroit et au bon moment. Ces sites comprennent les centres d’organisation des microtubules (MTOC), tels que les centrosomes pendant la mitose ou le Golgi dans les fibroblastes en migration, les côtés de microtubules préexistants ou des régions spécialisées du cytoplasme, telles que le cytosol entourant la chromatine mitotique. Une fois générés, les moteurs moléculaires peuvent faire glisser les microtubules les uns contre les autres ou même guider la direction de la croissance des microtubules. Les microtubules peuvent également être stabilisés par des modifications post-traductionnelles ou par la liaison d’autres protéines. Bien que n’étant pas un objectif du laboratoire, nous nous intéressons également à ces processus post-nucléés car, collectivement, ils sont importants pour la formation correcte des réseaux de microtubules.
Principaux domaines de recherche actuellement au sein du laboratoire
- Étude des mécanismes moléculaires régulant le recrutement et l’activation des γ-TuRC dans différents MTOC
- Comprendre comment la formation et la polarité des microtubules sont régulées dans les neurones.
Méthodologie
Nous utilisons principalement la drosophile comme système modèle animal multicellulaire in vivo. Nous combinons une manipulation précise du génome, une imagerie cellulaire avancée fixe et vivante et des tests biochimiques pour sonder la régulation moléculaire des microtubules et l’effet de leur mauvaise régulation dans les cellules.
Impact
Nos travaux ont des implications pour le cancer et les maladies neurodégénératives, car les γ-TuRC ont été identifiés comme des cibles anticancéreuses potentielles et les microtubules font partie d’une réponse importante lors d’un stress neuronal.

Membres
 Isabelle BECAM, Assistant Professor, CONDUIT LAB+33 (0)1 57 27 80 95, bureau 457B
Isabelle BECAM, Assistant Professor, CONDUIT LAB+33 (0)1 57 27 80 95, bureau 457B Abir ELFARKOUCHI, PhD student, CONDUIT LAB+33 (0)1 57 27 80 95, bureau 457B
Abir ELFARKOUCHI, PhD student, CONDUIT LAB+33 (0)1 57 27 80 95, bureau 457B Silvia-Maria Gonzalez-Martinez, Intern, CONDUIT LAB
Silvia-Maria Gonzalez-Martinez, Intern, CONDUIT LAB Cecile HU, PhD student, CONDUIT LABbureau 457B
Cecile HU, PhD student, CONDUIT LABbureau 457B Léane LEMOUR, Intern, CONDUIT LAB
Léane LEMOUR, Intern, CONDUIT LAB Léa MAMMRI, Biology engineer, CONDUIT LAB+33 (0)1 57 27 80 08, bureau 457B
Léa MAMMRI, Biology engineer, CONDUIT LAB+33 (0)1 57 27 80 08, bureau 457B Horgan Manirakiza, Postdoctoral researcher, CONDUIT LAB
Horgan Manirakiza, Postdoctoral researcher, CONDUIT LAB Akila MERAH, Postdoctoral researcher, CONDUIT LAB+33 (0)1 57 27 80 95, bureau 457B
Akila MERAH, Postdoctoral researcher, CONDUIT LAB+33 (0)1 57 27 80 95, bureau 457B Caina NING, Postdoctoral researcher, CONDUIT LAB
Caina NING, Postdoctoral researcher, CONDUIT LAB Anaelle TAIEB, PhD student, CONDUIT LAB+33 (0)1 57 27 80 95, bureau 457B
Anaelle TAIEB, PhD student, CONDUIT LAB+33 (0)1 57 27 80 95, bureau 457B Cléophée VAN MAELE, Biology engineer, CONDUIT LAB
Cléophée VAN MAELE, Biology engineer, CONDUIT LAB Chithran VINEETHAKUMARI, Postdoctoral researcher, CONDUIT LAB+33 (0)1 57 27 80 95, bureau 457B
Chithran VINEETHAKUMARI, Postdoctoral researcher, CONDUIT LAB+33 (0)1 57 27 80 95, bureau 457B
Pour contacter un membre de l’équipe par mail : prenom.nom@ijm.fr
Publications
- Impulscience, Fondation Bettencourt-Schueller
- ANR project grant
- IDex, Université Parix Cité
21.11.2023 : Prix Impulscience 2023
Nous sommes toujours à la recherche de postdocs talentueux qui s’intéressent de près à la régulation des microtubules. Si vous souhaitez rejoindre l’équipe, envoyez à Paul Conduit un CV et une lettre de motivation expliquant pourquoi vous souhaitez rejoindre l’équipe et désignant deux personnes de référence.


