Institut Jacques Monod
Unité mixte de recherche CNRS | Université Paris Cité
Un institut international de recherche en biologie fondamentale
Actualités
Les prochains événements
Séminaire de l’Institut Jacques Monod – Laurent Blanchoin & Manuel Théry
Paris
12 juin 2026 11:00
En savoir plus
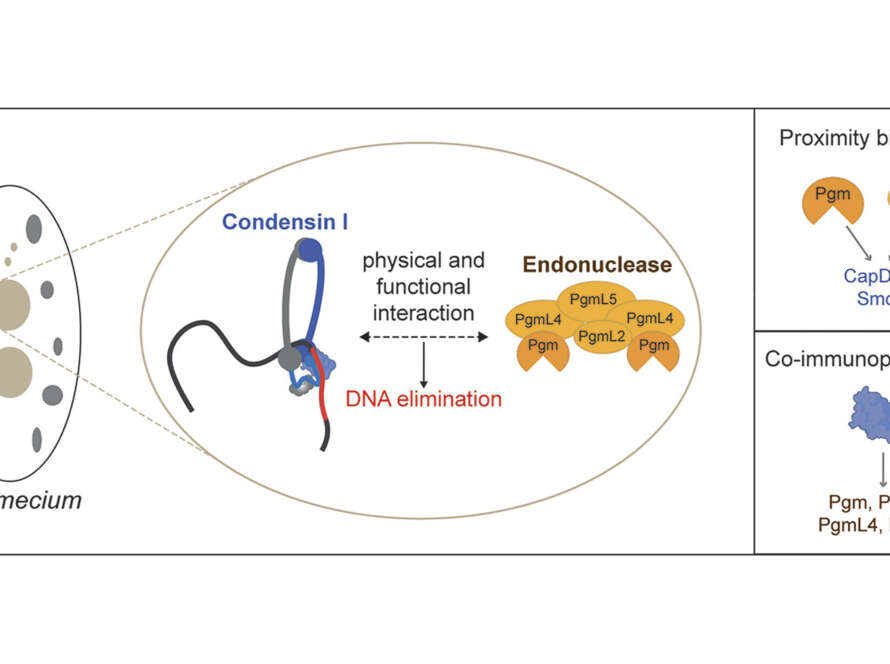
Conférence Jacques Monod – The mechanistic and evolutionary basis of programmed DNA elimination
Roscoff
21 septembre 2026-25 septembre 2026
En savoir plus
Les dernières publications
Equipes
0
Chercheurs et Enseignants-Chercheurs
0
Post-Docs
0
Doctorants
0
Ingénieurs Techniciens Administratifs
0
Nationalités
0