Plateforme ProteoSeine de l’Institut Jacques Monod
ProteoSeine est la plateforme protéomique de l’Institut Jacques Monod, UMR 7592 Université de Paris Cité – CNRS. Elle est localisée depuis début 2009 dans le bâtiment Buffon au 15 rue Hélène Brion, 75205 Paris CEDEX 13 – France. Les activités de la plateforme incluent du service analytique, de la recherche et du développement technique et méthodologique ainsi qu’une veille technologique active. Dans ce contexte, elle utilise les approches les plus modernes de la spectrométrie de masse pour l’étude des constituants protéiques des systèmes vivants.
Sa mission est d’offrir à la communauté des chercheurs en biologie des compétences et services à l’état de l’art permettant d’intégrer des approches protéomiques dans le développement de leurs projets scientifiques.
ProteoSeine peut appuyer sa R&D sur les recherches actives en biologie fondamentale des équipes de l’Institut Jacques Monod, sur des collaborations avec le milieu hospitalier et sur un long savoir-faire en développement analytique de protéines thérapeutiques. L’équipe développe particulièrement son expertise dans l’analyse quantitative différentielle à haut débit de mélanges protéiques complexes, l’analyse de modifications post-traductionnelles, la caractérisation de protéines pharmaceutiques recombinantes et l’analyse de complexes non-covalents par spectrométrie de masse en conditions natives. Des approches de type bottom-up et top-down à l’échelle nano ou capillaire sont utilisées en fonction des problématiques rencontrées.
La plateforme est labellisée par le GIS IBiSA (Infrastructures pour la Biologie, la Santé et l’Agronomie) et par le Cancéropôle Ile-de-France. Elle est ouverte à l’ensemble de la communauté scientifique nationale et internationale, publique et privée. La traçabilité des activités est assurée via l’enregistrement des prestations et des utilisateurs dans un LIMS spécialement développé en interne et les données brutes sont stockées en redondance via une solution gérée globalement par l’Institut Jacques Monod.
ProteoSeine est également membre associé de ProFi, l’infrastructure nationale de recherche dédiée à l’analyse protéomique et bénéficie du soutien des organismes suivants :

ProteoSeine assure la mise en œuvre de spectromètres de masse haute résolution de type électrospray couplés à des systèmes chromatographiques à haute performance.
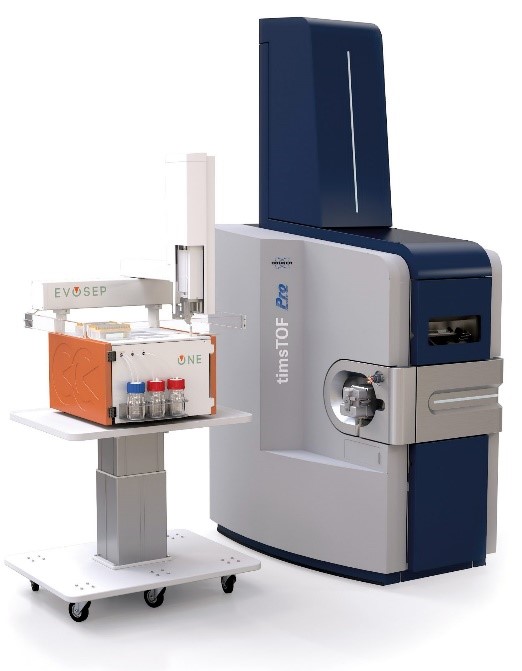
Les analyses bottom-up sont réalisées sur un appareil de dernière génération de type timsTOF Pro2 (Bruker) couplé à un automate de séparation haut débit (Evosep One). La technologie de mobilité ionique TIMS (Trapped Ion Mobility Spectrometry) est avant tout une technique de séparation en phase gazeuse qui résout la complexité de l’échantillon grâce à une dimension supplémentaire de séparation en plus de la chromatographie liquide à haute performance et de la spectrométrie de masse. Le dispositif TIMS accumule et concentre également les ions d’un m/z et d’une mobilité donnée. En synchronisant les cycles d’accumulation et de séquençage des ions en parallèle (technologie PASEF, Parallel Accumulation–Serial Fragmentation), l’appareil peut offrir une vitesse et une sensibilité MS/MS extrêmement élevées pour une couverture approfondie du protéome et la quantification différentielle non-biaisée de protéines.
La plateforme est équipée de logiciels propriétaires permettant le retraitement des données brutes sur deux serveurs de calcul multicœurs et l’analyse statistique multivariée des résultats d’abondance. La plateforme est particulièrement en capacité de prendre en charge de larges quantités d’échantillons dans des workflows automatisés.
Les analyses en MS-native et sur protéine intacte sont réalisées sur un instrument de type Cyclic IMS (Waters) embarquant une technologie révolutionnaire de mobilité ionique cyclique. L’instrument est également doté de capacités de fragmentation EXD et SID en surcroît du mode de fragmentation CID disponible dans les cellules TRAP et TRANSFER. Cet instrument est couplé à une chaîne chromatographique capillaire haute pression de type M-Class ou Acquity Premier pour le développement de séparations haute résolution de protéines. Un robot nanomate ADVION est également disponible pour des analyses nanospray en infusion directe automatisée.

ProteoSeine dispose également d’une plateforme Hamilton pour la préparation automatisée d’échantillons et d’un système chromatographique haute pression pour la prise en charge de séparations de protéines suivant différentes modalités.

La plateforme assure la mise en œuvre de spectromètres de masse haute résolution de type électrospray couplés à des systèmes chromatographiques à haute performance. L’instrumentation et les outils bio-informatiques mis en place sont spécialement sélectionnés pour délivrer des résultats dans l’état de l’art de l’analyse protéomique.
La plateforme propose différents protocoles d’analyses sur des protéines intactes (top-down) ou après digestion (bottom-up) qui permettent notamment d’aborder les problématiques suivantes :
- Identification de protéines sur gel ou en solution
- Caractérisation de modifications post-traductionnelles (PTMs)
- Caractérisation de protéines recombinantes (Coverage, PTMs, process & product-related impurities, size or charge variants)
- Recherche de partenaires (Pull-Down)
- Recherche de biomarqueurs
- Analyse quantitative des variations d’abondance de protéomes (Label-Free)
- Analyse de protéomes spécifiques après enrichissement (ex : phosphoprotéome)
- Analyse de complexes par MS en conditions natives
Le principe de fonctionnement est dans un premier temps de contacter la plateforme pour définir un protocole d’analyse adapté au projet. Une fiche utilisateur précisant le fonctionnement de la plateforme sera transmise (également disponible dans la rubrique « documents »). Préalablement à toute analyse, cette fiche doit être retournée complétée avec les informations demandées. Dans un second temps, il suffit de prendre rendez-vous pour déposer les échantillons du mardi au jeudi afin de pouvoir les traiter dans les meilleurs délais.
Les résultats générés sont envoyés par e-mail dans un délai de 2 semaines en général pour des approches classiques et sont archivés. Les données brutes sont transmises à la demande car leur stockage et intégrité sont assurés par la plateforme de façon non-contractuelle. Après réception des résultats, l’utilisateur est donc responsable de l’intégrité de l’ensemble de ses données.
La tarification des prestations de la plateforme est calculée sur la base des coûts complet selon le référentiel DSFIM-SBOR-D-2014-46 du CNRS. Trois tarifications distinctes sont appliquées selon l’origine de l’émetteur du bon de commande, c’est à dire CNRS/UPC, autre académique et enfin privé. Les tarifs ci-dessous sont exprimés hors taxe ; ils sont à majorer de la TVA au taux en vigueur.
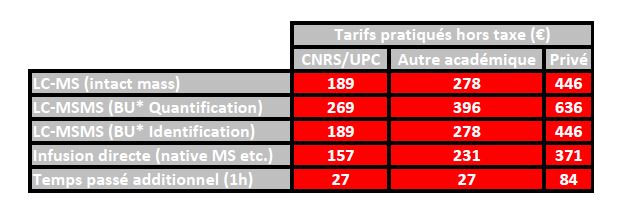
Tarification en vigueur depuis le 9 Avril 2021. * BU Bottom-Up
Les unités mixtes UPC/INSERM en délégation global de gestion INSERM listées ci-dessous bénéficient néanmoins du tarif CNRS/UPC.
| UMR | Directeur | Intitulé | Implantation |
| U942 | Alain Cohen-Solal | Biomarqueurs cardio-neuro-vasculaires : BIO-CANVAS | Hôpital Lariboisière |
| U958 | Cécile Julier | Génétique des diabètes | Faculté médecine UP |
| U965 | Marc Pocard | CARCINOSE angiogenèse et recherche transactionnelle : CART | Hôpital Lariboisière |
| U1131 | Stephane GIRAUDIER | Hématopoïèse normale et pathologique : émergence, environnement et recherche translationnelle | Hôpital Saint-Louis |
| U976 | Armand Bensussan | HIPI « Immunologie Humaine, Pathophysiologie, Immunothérapie » | Hôpital Saint-Louis |
| U1160 | Antoine Toubert | Écotaxie, micro-environnement et développement lymphocytaire | Hôpital Saint-Louis |
| U944 | Jean Soulier | Génomes, biologie cellulaire et thérapeutique | Hôpital Saint-Louis |
| U1123 | Corinne Alberti | Epidémiologie clinique et évaluation économique appliquées aux populations vulnérables : ECEVE | Faculté médecine UP |
| U1132 | Martine Cohen-Solal | Biologie de l’os et du cartilage : régulations et ciblage thérapeutique : BIOSCAR | Hôpital Lariboisière |
| U1134 | Yves Collin | Biologie intégrée du globule rouge | INTS |
| U1137 | Erik Denamur | Infection, antimicrobiens, modélisation, évolution : IAME | Faculté Bichat |
| U1141 | Pierre Gressens | Neuroprotection du cerveau en développement : PROTECT | Hôpital Robert Debré |
| U1148 | Didier Letourneur | Laboratoire de recherche vasculaire transactionnelle | Faculté Bichat |
| U1149 | Renato Monteiro | Centre de recherche sur l’inflammation : CRI | Faculté Bichat |
| U1152 | Marina Pretolani | Physiopathologie et épidémiologie des maladies respiratoires | Faculté Bichat |
| U1161 | Elisabeth Tournier-Lasserve | Génétique et physiopathologie des maladies cérébro-vasculaires | Faculté médecine UP |
L’équipe de ProteoSeine est fortement impliquée dans des actions de formation initiale et continue.
Elle dispense chaque année une semaine de formation théorique et pratique de l’analyse protéomique par spectrométrie de masse aux étudiants du M2-Pro « Ingénierie de Plateforme » d’Université Paris Cité.
Elle accueille tous les ans un étudiant de niveau M2 pour son stage pratique de fin d’études d’une durée de 6 mois.
Elle organise une formation à la spectrométrie de masse en protéomique quantitative et caractérisation de protéines recombinantes. Cette formation est référencée au catalogue de CNRS Formation Entreprise.
Elle organise 2 workshops internationaux par an dans le cadre du programme européen Twinning H2020 « MiCoBion »
Contact plateforme :
spectrodemasse@ijm.fr, +33 (0)1 57 27 81 82
Responsable
 Guillaume CHEVREUX, ProtéoSeine proteomics facility manager, PFT/PROTEOSEINE+33 (0)1 57 27 81 19, bureau 657B
Guillaume CHEVREUX, ProtéoSeine proteomics facility manager, PFT/PROTEOSEINE+33 (0)1 57 27 81 19, bureau 657B
Membres
 Jean-Baptiste BOYER, Proteomics engineer, PFT/PROTEOSEINE+33 (0)1 57 27 81 82, bureau 657B
Jean-Baptiste BOYER, Proteomics engineer, PFT/PROTEOSEINE+33 (0)1 57 27 81 82, bureau 657B Jean-Michel CAMADRO, Emeritus researcher, PFT/PROTEOSEINE+33 (0)1 57 27 80 95, bureau 344B
Jean-Michel CAMADRO, Emeritus researcher, PFT/PROTEOSEINE+33 (0)1 57 27 80 95, bureau 344B Victor COCHARD, Proteomics engineer, PFT/PROTEOSEINE+33 (0)1 57 27 81 82, bureau 657B
Victor COCHARD, Proteomics engineer, PFT/PROTEOSEINE+33 (0)1 57 27 81 82, bureau 657B Veronique LEGROS, Proteomics engineer, PFT/PROTEOSEINE+33 (0)1 57 27 81 82, bureau 657B
Veronique LEGROS, Proteomics engineer, PFT/PROTEOSEINE+33 (0)1 57 27 81 82, bureau 657B
Pour contacter un membre de l’équipe par mail : prenom.nom@ijm.fr
Plateforme ProteoSeine de l’Institut Jacques Monod, Bâtiment Buffon – Aile B, Pièce 657B, 6e étage – 15 rue Hélène Brion – 75205 Paris Cedex 13 – FRANCE
Charte utilisateur
4202101_Fiche Utilisateur ProteoSeine_2022
Minimiser les contaminations pour l’analyse protéomique
Minimizing contamination in Proteomics
Protocoles de lyse cellulaire pour l’analyse protéomique
Publications en co-auteur avec des membres de l’établissement (2021-2025)
2025
de Oliveira Formiga R, Li Q, Zhao Y, Campos Ribeiro MA, Guarino-Vignon P, Fatouh R, Dubois L, Creusot L, Puchois V, Amouyal S, Alonso Salgueiro I, Bredon M, Chollet L, Ledent T, Scandola C, Auger JP, Danne C, Krönke G, Tkacz E, Emond P, Chevreux G, Pham HP, Pontoizeau C, Lamaziere A, Argüello RJ, Rolhion N, Michel ML, Wai T, Sokol H. Immunometabolic reprogramming of macrophages by gut microbiota-derived cadaverine controls colon inflammation. Cell Host Microbe. 2025 Sep 30:S1931-3128(25)00375-0. doi: 10.1016/j.chom.2025.09.009.
Li Q, de Oliveira Formiga R, Puchois V, Creusot L, Ahmad AH, Amouyal S, Campos-Ribeiro MA, Zhao Y, Harris DMM, Lasserre F, Ellero-Simatos S, Guillou H, Huang Z, Brot L, Hu Y, Chollet L, Danne C, Scandola C, Ledent T, Chevreux G, Argüello RJ, De Carvalho Bittencourt M, Bettinger J, D’Aveni-Piney M, Moulin D, Schreiber S, Aden K, Rolhion N, Michel ML, Wai T, Sokol H. Microbial metabolite indole-3-propionic acid drives mitochondrial respiration in CD4+ T cells to confer protection against intestinal inflammation. Nat Metab. 2025 Oct 21. doi: 10.1038/s42255-025-01396-6.
Mérida-Cerro JA, Chevreux G, Palancade B, Rondón AG, Aguilera A. Cellular imbalance of specific RNA-binding proteins associates with harmful R-loops. PLoS Genet. 2025 Jul 2;21(7):e1011491. doi: 10.1371/journal.pgen.1011491.
Roumbo L, Ossareh-Nazari B, Vigneron S, Stefani I, Van Hove L, Legros V, Chevreux G, Lacroix B, Castro A, Joly N, Lorca T, Pintard L. The MAST kinase KIN-4 carries out mitotic entry functions of Greatwall in C. elegans. EMBO J. 2025 Apr;44(7):1943-1974. doi: 10.1038/s44318-025-00364-w.
Cui G, Ley M, Mechaly AE, Bui LC, Michail C, Berthelet J, Dairou J, Yang H, Chevreux G, Moroy G, Green MR, Haouz A, Rodrigues Lima F. Structural and functional characterization of CREB-binding protein (CREBBP) as a histone propionyltransferase. J Biol Chem. 2025 Aug;301(8):110444. doi: 10.1016/j.jbc.2025.110444.
Charmant O, Gruchota J, Arnaiz O, Nowak KP, Moisan N, Zangarelli C, Bétermier M, Anielska-Mazur A, Legros V, Chevreux G, Nowak JK, Duharcourt S. The PIWI-interacting protein Gtsf1 controls the selective degradation of small RNAs in Paramecium. Nucleic Acids Res. 2025 Jan 7;53(1):gkae1055. doi: 10.1093/nar/gkae1055.
Bellaye PS, Georgievski A, Ballerini P, Bouslama B, Richard C, Boidot R, Chevreux G, Legros V, Guy J, Racine J, Collin B, Garrido C, Quéré R. CD40 Agonist on Patient-Derived Xenograft Mice for the Treatment of B-Cell Acute Lymphoblastic Leukemia. Clin Cancer Res. 2025 Jan 6;31(1):181-196. doi: 10.1158/1078-0432.CCR-24-1391.
Miró-Pina C, Charmant O, Giovannetti M, de Vanssay A, Frapporti A, Humbert A, Lhuillier-Akakpo M, Chevreux G, Arnaiz O, Duharcourt S. A histone methyltransferase-independent function of PRC2 controls small RNA dynamics during programmed DNA elimination in Paramecium. Nucleic Acids Res. 2025 Oct 14;53(19):gkaf1048. doi: 10.1093/nar/gkaf1048.
Cruz-Gamero JM, Ballardin D, Lecis B, Zhang CL, Cobret L, Gast A, Morisset-Lopez S, Piskorowski R, Langui D, Jose J, Chevreux G, Rebholz H. Missense mutation in the activation segment of the kinase CK2 models Okur-Chung neurodevelopmental disorder and alters the hippocampal glutamatergic synapse. Mol Psychiatry. 2025 Apr;30(4):1497-1509. doi: 10.1038/s41380-024-02762-8.
Ženíšková K, Stopka P, Martín-Pérez T, Chevreux G, Grechnikova M, Drncová E, Malych R, Mach J, Walochnik J, Camadro JM, Sutak R. Molecular Mechanisms of Acanthamoeba castellanii Response to Different Sources of Oxidative Stress. J Proteome Res. 2025 Feb 7;24(2):449-458. doi: 10.1021/acs.jproteome.4c00573.
Ballin A, Albanèse V, Miled S, Legros V, Chevreux G, Verraes A, Friedrich A, Léon S. A genetic screen reveals a key role for Reg1 in 2-deoxyglucose sensing and yeast AMPK inhibition. PLoS Genet. 2025 Oct 9;21(10):e1011896. doi: 10.1371/journal.pgen.1011896.
2024
Safieddine A, Benassy MN, Bonte T, Slimani F, Pourcelot O, Kress M, Ernoult-Lange M, Courel M, Coleno E, Imbert A, Laine A, Godebert AM, Vinit A, Blugeon C, Chevreux G, Gautheret D, Walter T, Bertrand E, Bénard M, Weil D. Cell-cycle-dependent mRNA localization in P-bodies. Mol Cell. 2024 Nov 7;84(21):4191-4208.e7. doi: 10.1016/j.molcel.2024.09.011.
Boismal F, Peltier S, Ly Ka So S, Chevreux G, Blondel L, Serror K, Setterblab N, Zuelgaray E, Boccara D, Mimoun M, Guere C, Benssussan A, Dorr M, Beauchef G, Vie K, Michel L. Proteomic and secretomic comparison of young and aged dermal fibroblasts highlights cytoskeleton as a key component during aging. Aging (Albany NY). 2024 Aug 27;16(16):11776-11795. doi: 10.18632/aging.206055.
Wiedemann A, Oussalah A, Guéant Rodriguez RM, Jeannesson E, Merten M, Rotaru I, Alberto JM, Baspinar O, Rashka C, Hassan Z, Siblini Y, Matmat K, Jeandel M, Chery C, Robert A, Chevreux G, Lignières L, Camadro JM, Hergalant S, Feillet F, Coelho D, Guéant JL. Multiomic analysis in fibroblasts of patients with inborn errors of cobalamin metabolism reveals concordance with clinical and metabolic variability. EBioMedicine. 2024 Jan;99:104911. doi: 10.1016/j.ebiom.2023.104911. Erratum in: EBioMedicine. 2025 Feb;112:105540. doi: 10.1016/j.ebiom.2024.105540.
Zheng Y, Cabassa-Hourton C, Eubel H, Chevreux G, Lignieres L, Crilat E, Braun HP, Lebreton S, Savouré A. Pyrroline-5-carboxylate metabolism protein complex detected in Arabidopsis thaliana leaf mitochondria. J Exp Bot. 2024 Feb 2;75(3):917-934. doi: 10.1093/jxb/erad406. PMID: 37843921.
Villares M, Lourenço N, Ktorza I, Berthelet J, Panagiotou A, Richard A, Amo A, Koziy Y, Medjkane S, Valente S, Fioravanti R, Pioche-Durieu C, Lignière L, Chevreux G, Mai A, Weitzman JB. Theileria parasites sequester host eIF5A to escape elimination by host-mediated autophagy. Nat Commun. 2024 Mar 12;15(1):2235. doi: 10.1038/s41467-024-45022-7.
Celebic D, Polat I, Legros V, Chevreux G, Wassmann K, Touati SA. Qualitative rather than quantitative phosphoregulation shapes the end of meiosis I in budding yeast. EMBO J. 2024 Apr;43(7):1325-1350. doi: 10.1038/s44318-024-00032-5.
Labarre C, Zhang Y, Lesur E, Ley M, Sago L, Dietrich C, de Sousa-d’Auria C, Constantinesco-Becker F, Baron A, Doisneau G, Urban D, Chevreux G, Guianvarc’h D, Bourdreux Y, Bayan N. Bioorthogonal Monomycolate of Trehalose Disclosed the O-Mycoloylation of Mycoloyltransferases and Other Cell Envelope Proteins in C. glutamicum. ACS Chem Biol. 2024 Nov 15;19(11):2359-2371. doi: 10.1021/acschembio.4c00502.
2023
Scrima N, Le Bars R, Nevers Q, Glon D, Chevreux G, Civas A, Blondel D, Lagaudrière-Gesbert C, Gaudin Y. Rabies virus P protein binds to TBK1 and interferes with the formation of innate immunity-related liquid condensates. Cell Rep. 2023 Jan 31;42(1):111949. doi: 10.1016/j.celrep.2022.111949.
Gareil N, Gervais A, Macaisne N, Chevreux G, Canman JC, Andreani J, Dumont J. An unconventional TOG domain is required for CLASP localization. Curr Biol. 2023 Aug 21;33(16):3522-3528.e7. doi: 10.1016/j.cub.2023.07.009.
Trouillard O, Dupaigne P, Dunoyer M, Doulazmi M, Herlin MK, Frismand S, Riou A, Legros V, Chevreux G, Veaute X, Busso D, Fouquet C, Saint-Martin C, Méneret A, Trembleau A, Dusart I, Dubacq C, Roze E. Congenital mirror movements are associated with defective polymerisation of RAD51. J Med Genet. 2023 Nov;60(11):1116-1126. doi: 10.1136/jmg-2023-109189.
Nashed S, El Barbry H, Benchouaia M, Dijoux-Maréchal A, Delaveau T, Ruiz-Gutierrez N, Gaulier L, Tribouillard-Tanvier D, Chevreux G, Le Crom S, Palancade B, Devaux F, Laine E, Garcia M. Functional mapping of N-terminal residues in the yeast proteome uncovers novel determinants for mitochondrial protein import. PLoS Genet. 2023 Aug 16;19(8):e1010848. doi: 10.1371/journal.pgen.1010848.
Nkombo Nkoula S, Velez-Aguilera G, Ossareh-Nazari B, Van Hove L, Ayuso C, Legros V, Chevreux G, Thomas L, Seydoux G, Askjaer P, Pintard L. Mechanisms of nuclear pore complex disassembly by the mitotic Polo-like kinase 1 (PLK-1) in C. elegans embryos. Sci Adv. 2023 Jul 21;9(29):eadf7826. doi: 10.1126/sciadv.adf7826.
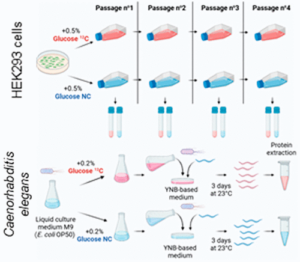
Lignieres L, Sénécaut N, Dang T, Bellutti L, Hamon M, Terrier S, Legros V, Chevreux G, Lelandais G, Mège RM, Dumont J, Camadro JM. Extending the Range of SLIM-Labeling Applications: From Human Cell Lines in Culture to Caenorhabditis elegans Whole-Organism Labeling. J Proteome Res. 2023 Mar 3;22(3):996-1002. doi: 10.1021/acs.jproteome.2c00699.
Bayot J, Martin C, Chevreux G, Camadro JM, Auchère F. The adaptive response to alternative carbon sources in the pathogen Candida albicans involves a remodeling of thiol- and glutathione-dependent redox status. Biochem J. 2023 Feb 14;480(3):197-217. doi: 10.1042/BCJ20220505.
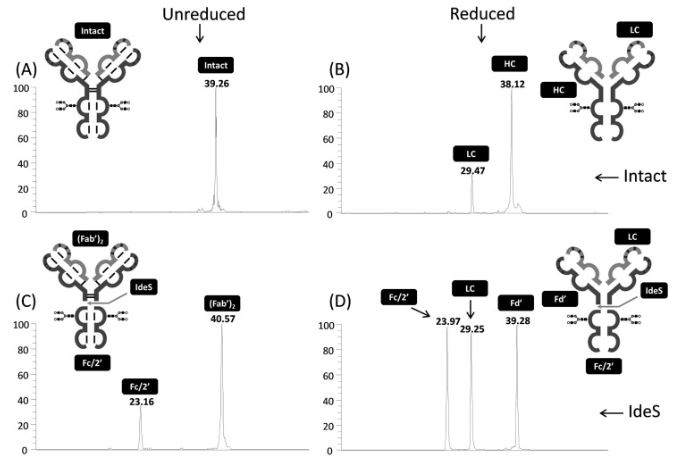
Lignieres L, Legros V, Khelil M, Senecaut N, Lauber MA, Camadro JM, Chevreux G. Capillary liquid chromatography coupled with mass spectrometry for analysis of nanogram protein quantities on a wide-pore superficially porous particle column in top-down proteomics. J Chromatogr B Analyt Technol Biomed Life Sci. 2023 Jan 1;1214:123566. doi: 10.1016/j.jchromb.2022.123566
2022
Protein Kinase CK2 Acts as a Molecular Brake to Control NADPH Oxidase 1 Activation and Colon Inflammation Dan Liu, Jean-Claude Marie, Anne-Laure Pelletier, Zhuoyao Song, Marwa Ben-Khemis, Kaouthar Boudiaf, Coralie Pintard, Thibaut Leger, Samuel Terrier, Guillaume Chevreux, Jamel El-Benna, Pham My-Chan Dang Cell Mol Gastroenterol Hepatol. 2022;13(4):1073-1093. DOI:10.1016/j.jcmgh.2022.01.003, PMID: 35031518
Paramecium Polycomb repressive complex 2 physically interacts with the small RNA-binding PIWI protein to repress transposable elements. Miró-Pina C, Charmant O, Kawaguchi T, Holoch D, Michaud A, Cohen I, Humbert A, Jaszczyszyn Y, Chevreux G, Del Maestro L, Ait-Si-Ali S, Arnaiz O, Margueron R, Duharcourt S. Dev Cell. 2022 Apr 25;57(8):1037-1052.e8. doi: 10.1016/j.devcel.2022.03.014. Epub 2022 Apr 15. PMID: 35429435
Quantitative Proteomics in Yeast: From bSLIM and Proteome Discoverer Outputs to Graphical Assessment of the Significance of Protein Quantification Scores. Sénécaut N, Poulain P, Lignières L, Terrier S, Legros V, Chevreux G, Lelandais G, Camadro JM. Methods Mol Biol. 2022;2477:275-292. doi: 10.1007/978-1-0716-2257-5_16. PMID: 35524123
Cisplatin causes covalent inhibition of protein-tyrosine phosphatase 1B (PTP1B) through reaction with its active site cysteine: Molecular, cellular and in vivo mice studies. Liu R, Zhang W, Gou P, Berthelet J, Nian Q, Chevreux G, Legros V, Moroy G, Bui LC, Wang L, Dupret JM, Deshayes F, Lima FR. Biomed Pharmacother. 2022 Jul 6;153:113372. doi: 10.1016/j.biopha.2022.113372. Online ahead of print. PMID: 35809481
The evolutionary conserved proteins CEP90, FOPNL, and OFD1 recruit centriolar distal appendage proteins to initiate their assembly. Le Borgne P, Greibill L, Laporte MH, Lemullois M, Bouhouche K, Temagoult M, Rosnet O, Le Guennec M, Lignières L, Chevreux G, Koll F, Hamel V, Guichard P, Tassin AM. PLoS Biol. 2022 Sep 7;20(9):e3001782. doi: 10.1371/journal.pbio.3001782. eCollection 2022 Sep.
Diverse susceptibilities and responses of human and rodent cells to orthohantavirus infection reveal different levels of cellular restriction. Gallo G, Kotlik P, Roingeard P, Monot M, Chevreux G, Ulrich RG, Tordo N, Ermonval M. PLoS Negl Trop Dis. 2022 Oct 12;16(10):e0010844. doi: 10.1371/journal.pntd.0010844. eCollection 2022 Oct.
2021
Fetal Programming by Methyl Donor Deficiency Produces Pathological Remodeling of the Ascending Aorta Balint B, Hergalan S, Camadro JM, Blaise S, Vanalderwiert L, Lignières L, Guéant-Rodriguez RM, Guéant JL. Arterioscler Thromb Vasc Biol. 2021 Apr 8;ATVBAHA120315587 doi: 10.1161/ATVBAHA.120.315587.
Co-translational assembly and localized translation of nucleoporins in nuclear pore complex biogenesis Lautier O, Penzo A, Rouvière J.O, Chevreux G, Collet L, Loïodice I, Taddei A, Devaux F, Collart MA, Palancade B. Mol Cell. 2021 Apr 4;S1097-2765(21)00225-2. doi: 10.1016/j.molcel.2021.03.030.
The M-phase regulatory phosphatase PP2A-B55δ opposes protein kinase A on Arpp19 to initiate meiotic division. Lemonnier T, Daldello EM, Poulhe R, Le T, Miot M, Lignières L, Jessus C, Dupré A. Nat Commun. 2021 Mar 23;12(1):1837. doi: 10.1038/s41467-021-22124-0. PMID: 33758202
Novel Insights into Quantitative Proteomics from an Innovative Bottom-Up Simple Light Isotope Metabolic (bSLIM) Labeling Data Processing Strategy. Sénécaut N, Alves G, Weisser H, Lignières L, Terrier S, Yang-Crosson L, Poulain P, Lelandais G, Yu YK, Camadro JM. J Proteome Res. 2021 Mar 5;20(3):1476-1487. doi: 10.1021/acs.jproteome.0c00478. Epub 2021 Feb 11. PMID: 33573382
Isoginkgetin derivative IP2 enhances the adaptive immune response against tumor antigens. Darrigrand R, Pierson A, Rouillon M, Renko D, Boulpicante M, Bouyssié D, Mouton-Barbosa E, Marcoux J, Garcia C, Ghosh M, Alami M, Apcher S. Commun Biol. 2021 Mar 1;4(1):269. doi: 10.1038/s42003-021-01801-2. PMID: 33649389
Interactions of Viral Proteins from Pathogenic and Low or Non-Pathogenic Orthohantaviruses with Human Type I Interferon Signaling. Gallo G, Caignard G, Badonnel K, Chevreux G, Terrier S, Szemiel A, Roman-Sosa G, Binder F, Gu Q, Da Silva Filipe A, Ulrich RG, Kohl A, Vitour D, Tordo N, Ermonval M. Viruses. 2021 Jan 19;13(1):140. doi: 10.3390/v13010140. PMID: 33478127
Bariatric surgery induces a new gastric mucosa phenotype with increased functional glucagon-like peptide-1 expressing cells. Ribeiro-Parenti L, Jarry AC, Cavin JB, Willemetz A, Le Beyec J, Sannier A, Benadda S, Pelletier AL, Hourseau M, Léger T, Morlet B, Couvelard A, Anini Y, Msika S, Marmuse JP, Ledoux S, Le Gall M, Bado A. Nat Commun. 2021 Jan 4;12(1):110. doi: 10.1038/s41467-020-20301-1. PMID: 33397977
15/06/2023 :
La plateforme ProtéoSeine organise un séminaire conjointement avec la société Protein Metrics. Ce séminaire aura pour but de présenter le travail effectué par la plateforme, notamment sur l’analyse de protéines intactes.
La société Protein Metrics présentera quant à elle ses différentes solutions logicielles, pour l’analyse de protéines, peptides et oligonucléotides.
Ce séminaire aura lieu dans la matinée du jeudi 15 juin 2023, à l’Institut Jacques Monod.
Envie de participer ?
Vous pouvez visionner le programme et vous inscrire ici : https://proteinmetrics.com/paris-symposium-2023/
06/02/2023
L’équipe de Jean-Michel Camadro en collaboration avec la plateforme ProtéoSeine, l’équipe Ladoux/Mège et Dumont viennent de publier un nouvel article :
Laurent Lignières, Nicolas Sénécaut, Tien Dang, Laura Bellutti, Marion Hamon, Samuel Terrier, Véronique Legros, Guillaume Chevreux, Gaëlle Lelandais, René-Marc Mège, Julien Dumont, and Jean-Michel Camadro, Journal of Proteome Research, 2023, 22, 3, 996–1002
07/02/2023
L’équipe de Jean-Michel Camadro en collaboration avec la plateforme ProtéoSeine viennent de publier un nouvel article :
Juliette Bayot, Caroline Martin, Guillaume Chevreux, Jean-Michel Camadro, Françoise Auchère, Biochemical Journal Volume 480, Issue 3.
05/01/2023 : la plateforme Protoseine vient de publier un nouvel article dans Journal of Chromatography B :
29/11/2022 : Inauguration de nouveaux équipements lors des 40 ans de l’IJM avec la Région Ile-de-France